Aras Innovatorで非常に困難な課題を解決している医療機器のリーダー
医療機器業界向けのベストインクラスの PLM 機能
豊富な Aras に特化した経験を持つ Aras のパートナーであったミネルバ社が Aras と合併したことにより、Aras プラットフォーム上で開発された医療機器業界向けのソリューションが利用可能となりました。持続的な DX は、グローバル企業にとって、市場投入期間の短縮、コンプライアンスの維持、および高品質な製品提供のために重要です。ミネルバ社の医療機器向けのビジネス アプリケーションは、DX をアジャイルに実現できるように設計されています。

Aras で構築する医療機器メーカー
医療機器メーカーにおける PLM のメリット
製品構想から市場投入、廃棄まで、製品ライフサイクル全体を通して医療機器メーカーが直面する課題は大きく、部門を超えて多くのプロセスや社外のサプライヤーにまで関わります。製品ライフサイクル管理(PLM)がこれらの課題を克服し、より効率化を可能にする方法をご紹介します。

ケアストリーム社
医療業界の世界的リーディングカンパニーであるケアストリームヘルス社は、Aras プラットフォームでプロジェクトと機器履歴簿(DHF)を管理しています。 彼らがどのようにしてコストを削減し、市場投入までの時間を短縮し、規制遵守を達成したかをご覧ください。
ドレーゲル社の DX
デジタルトランスフォーメーションの取り組みの一環として、医療と安全技術の分野で世界トップクラスの企業であるドレーゲル社は、Oracle Agile e6 を Aras Innovator にリプレイスしました。
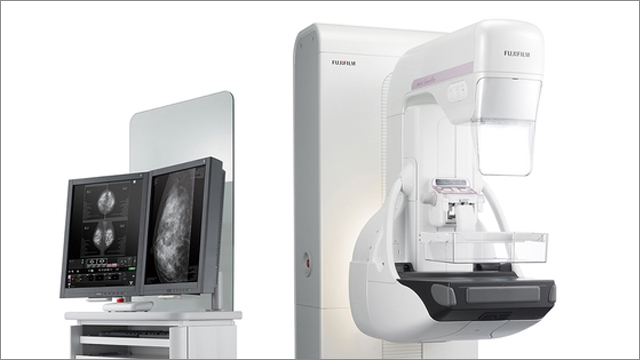
富士フイルム社
デジタルトランスフォーメーションの取り組みの一環として、医療と安全技術の分野で世界トップクラスの企業であるドレーゲル社は、Oracle Agile e6 を Aras Innovator にリプレイスしました。
ミネルバ社と Aras が提供するツールが業務を非常に簡単にするという事実がわかると、ユーザーは新しいシステムにすばやく順応します。 Aras Innovator と Minerva Medical Device PLM の組み合わせで、非常に使いやすくてわかりやすいソリューションになりました。その結果ユーザーから、今すぐ使えるほど簡単である、というフィードバックを受けました。機能の利便性はますます高まり、ユーザーはシステムでの作業に非常に満足しています。
Own the Lifecycle
製品とサービスを提供する各企業は、アフターサービスや製品の利用状況などを含めた製品の運用ライフサイクルに関するより多くの情報を求め、うまくコントロールしたいと考えています。これは、より持続可能なビジネス価値を創出する、持続可能な製品を開発するためです。Own the Lifecycle、デジタルスレッド、デジタルツインにフォーカスした、Aras のブログから洞察を得ることができます。